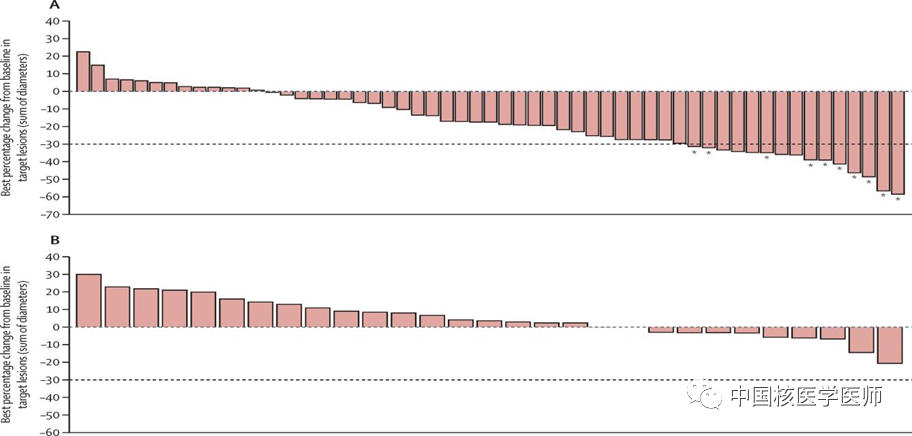
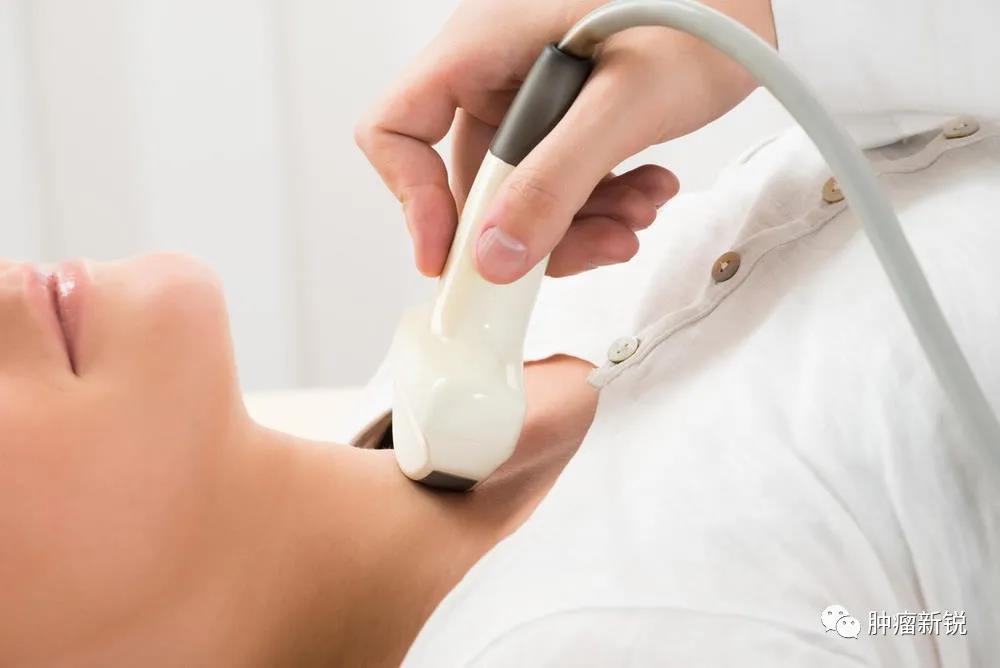
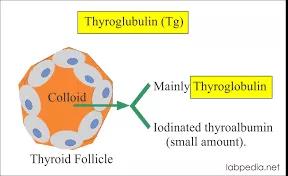
北京大学第三医院 乐云逸 翻译,王海宁 审校 Source:Carole Ann Spencer. Thyroid. 2023 Apr;33:407−419. 背景:本篇综述以时间轴形式,展现了过去七十年来技术进步如何影响甲状腺实验室检查的发展。 概要:甲状腺实验室检查从在核医学实验室使用同位素标记的碘(131碘和此后的125碘)作为信号的耗时的人工操作,演变为在常规临床化学实验室的多组分分析仪上进行的自动化非同位素检测。1960年前后同位素放射免疫测定技术的发展,随后20世纪70年代中期单克隆抗体技术的出现,引领了非同位素免疫测定方法的发展,形成了当今甲状腺实验室检查的支柱。本文综述了各项甲状腺指标的测量方法的发展:总甲状腺素、总三碘甲腺原氨酸、直接法和间接估算法游离甲状腺激素(游离甲状腺素和游离三碘甲腺原氨酸)、促甲状腺激素(thyrotropin,TSH)、甲状腺自身抗体[甲状腺过氧化物酶、甲状腺球蛋白(thyroglobulin,Tg)和TSH受体自身抗体] 及Tg。尽管在敏感性和特异性方面取得了进步,但现今的甲状腺实验室检查仍然存在检测方法不同带来的报告数值差异的局限性,以及检测试剂的非特异性干扰和分析物自身抗体的干扰。 结论:甲状腺疾病累及约10%的美国人口,且大多在门诊治疗,并带来了60%的内分泌实验室检查。未来,希望能够消除干扰,同时检测的标准化/均质化将有助于推动建立通用的检测参考范围。 关键词:抗体和甲状腺球蛋白;甲状腺激素;促甲状腺激素 引言 引言甲状腺激素和甲状腺激素受体的分子作用 图1显示了过去70年来甲状腺实验室检查发展的历史里程碑,从早期的人工同位素方法到目前在高通量非同位素分析仪上进行的自动化检测。目前如此大量的甲状腺实验室检查反映了美国人群中甲状腺疾病的高患病率(>10%)[1]。其中超过75% 检测的是促甲状腺激素(thyrotropin,TSH),同时检测(25%)或不检测(50%) 游离甲状腺素(free thyroxine,fT4),造成每年花费约16亿美元[2,3]。 图1. 影响TSH、总甲状腺激素(TT4和TT3)、游离甲状腺激素间接估测值(fT4和fT3)、直接fT4、甲状腺抗体 TPOAb、TgAb和TRAb以及Tg检测方法发展的重大技术进展的时间轴。ED-ID- LC-MS/MS,平衡透析联合同位素稀释液相色谱串联质谱;fT3,游离三碘甲腺原氨酸;fT4,游离甲状腺素;ICMA,免疫化学发光法;ID-LC-MS/MS,同位素稀释液相色谱串联质谱;IRMA,免疫放射分析;LATS,长效甲状腺刺激物;LC-MS/MS,液相色谱串联质谱;PBI,蛋白结合碘;RIA,放射免疫分析;Tg,甲状腺球蛋白;TgAb,甲状腺球蛋白自身抗体;TPOAb,甲状腺过氧化物酶抗体;TRAb,促甲状腺激素受体抗体;TRH,促甲状腺激素释放激素;TSH,促甲状腺激素;TSHR,促甲状腺激素受体;TT3,总三碘甲腺原氨酸;TT4,总甲状腺素。 甲状腺激素检测 引言甲状腺激素和甲状腺激素受体的分子作用 图2显示了甲状腺激素代谢的复杂性,其中循环中所有T4来源于甲状腺,但三碘甲腺原氨酸(triiodothyronine,T3)只有约20% 来源于甲状腺。T3与甲状腺核受体亲和力最高——比T4高10倍,其T3的代谢产物Triac[4]同样具有一些代谢活性[5],但反T3(reverse T3,rT3)是无活性的[6]。T4是用于评估甲状腺状态的首选测量指标,这是由于所有T4来源于甲状腺组织,具有甲状腺组织特异性,并且即使T4水平发生波动时,T4转化为T3的外周组织脱碘酶活性受到严密地调控,以维持循环T3最适宜的水平[7,8]。 图2. 图中显示了T4在外周组织中如何代谢形成初始代谢物:T3和rT3以及其硫酸盐衍生物。T3进一步代谢为Triac(T3Ac)并脱碘生成T3和rT3共同代谢产物3,3’-T2。这些代谢途径由脱碘酶(1型5’-脱碘酶、2型5’-脱碘酶和3型5’-脱碘酶)和PST及LAAO酶共同催化。LAAO,L-氨基酸氧化酶;PST,磷酸硫基转移酶;rT3,反三碘甲腺原氨酸。 T3的检测对于鉴别甲状腺功能亢进症的病因是Graves病或甲状腺炎尤为有用,这是由于导致Graves病出现甲状腺毒症的TSH受体抗体(TSH receptorantibodies,TRAb)可刺激甲状腺分泌T3为主,导致T3/T4的比值高于甲状腺功能正常或甲状腺炎时的比值[9]。研究表明rT3在饥饿[10]和甲状腺功能正常的病态综合征(nonthyroidal illness,NTI)[11]时增加,最初传达了一个错误印象,即rT3也是甲状腺功能的指标。然而,在甲状腺功能正常的志愿者中进行的代谢研究表明rT3的升高是由于其代谢清除率降低,而不是T4生成增加,这否定了rT3检测的临床应用,除非在甲状腺激素敏感性降低和消耗性甲状腺功能减退的罕见情况下[13,14]。尽管如此,目前网页上仍然存在错误信息,鼓励一些人进行昂贵的rT3检测[15]。 总激素(总甲状腺素和总三碘甲腺原氨酸)和游离激素指标 目前,大多数TT4和TT3的检测都是在自动化平台上通过非同位素免疫分析法进行的[21,22]。虽然这些方法与同位素稀释液相色谱串联质谱(isotopedilutionliquid chromatography/tandem mass spectrometry,IDLC-MS/MS)检测TT4的标准方法相关,现有的TT4免疫检测方法存在不可接受的检测方法间高偏倚和高总变异系数(coefficients of variation,CV)[21,22]。 人们早就认识到,甲状腺激素主要与血浆蛋白结合,主要是甲状腺素结合球蛋白(thyroxine bindingglobulin,TBG),还有一些与转甲状腺素蛋白及白蛋白结合。因此,即使患者甲状腺功能正常,其总激素水平也可能因结合蛋白升高或降低而异常[23]。妊娠期的高TBG状态问题尤为显著,与先天性TBG缺乏或过多、急性和慢性NTI以及某些药物治疗(雄激素、苯妥英钠、肝素及依诺肝素钠)相关的疾病亦是如此[23]。先天性白蛋白异常(异常白蛋白血症或无白蛋白血症)也被发现可干扰TT4的检测,在某些情况下还可干扰TT3的检测[24,25]。 由于TT4检测对TBG的依赖性,产生了两步“游离激素指数”法,即使用“T3摄取”方法对总激素水平(TT4或TT3)进行数学“校正”,以纠正TBG异常[26]。这些T3摄取试验间接测定了血清TBG结合能力,即与甲状腺激素结合的“清除剂”(如树脂或T3抗体)摄取125碘-T3示踪剂的量。在高TBG状态下,TBG和清除剂之间对示踪剂的竞争有利于TBG与示踪剂结合,从而导致与清除剂结合的示踪剂较少(低125碘-T3摄取)。相反,在低TBG状态下,与TBG结合的125碘-T3较少,与清除剂结合的则较多(高125碘-T3摄取)。1991年,美国甲状腺协会将T3摄取试验重新命名为“甲状腺激素结合率(ThyroidHormone Binding Ratio,THBR)试验”[27]。 目前的THBR方法使用不同的清除剂、配方、计算方法和参考范围。由于实际原因,早期THBR 试验首选125碘-T3而非125碘-T4,因为T3对TBG的亲和力低于T4,导致清除剂摄取的同位素较多[28],需要更短的同位素计数时间。目前的THBR试验被称为“甲状腺素结合力测定”试验,主要使用自动化免疫制剂和非同位素信号来评估相对于设定值为1.00或40%的参考值的可用TBG结合位点[29]。 直接检测fT4 1988年,第一种直接检测fT4的方法是使用一种敏感的RIA 测定血清透析液中的T4水平[33]。在过去的十年中,平衡透析(equilibrium dialysis,ED)联合ID-LC-MS/MS(ED-ID-LC-MS/MS) 测定透析液中fT4已成为参考方法的首选[36]。然而,由于仪器成本高、技术复杂和报销问题,fT4的直接检测仍未被广泛应用。fT3的直接检测只能在用于进行科学研究的实验室进行。在常规临床化学实验室进行的大多数fT4和fT3检测都使用的自动化估测。 单次游离激素的估测(fT4和fT3) 一步法类似物检测 fT3和fT4的两步/反向滴定法检测 目前fT4和fT3的估测是基于这两种方法的不同设计构图。现今大多数多组分分析仪都使用自动化非同位素检测。然而,尽管经过了20多年的发展,这些检测方法仍然对先天性白蛋白异常[25]、碘化甲状腺氨酸自身抗体[41]、嗜异性抗体(heterophileantibodies,Hab)[41]非常敏感,并且受到一些检测试剂如生物素、链霉亲和素和钌抗体的干扰[41,42]。此外,相对于ED-ID-LC MS/MS参考方法,目前的fT4估测法存在显著的方法间偏倚和负偏倚[43]。这种方法间的差异导致无法为评估妊娠等情况设定通用的参考范围(图3)[44]。在未来,希望制造商将根据ED-ID-LC-MS/MS参考方法对其检测进行重新标准化。 图3. 汇总已发表的43项研究显示,使用不同方法(雅培、贝克曼、罗氏和西门子)在孕期各阶段检测的fT4参考上限和下限(2.5%~97.5%)。数据显示,正如所预期的一样,甲状腺受人绒毛膜促性腺激素的刺激在孕早期达到最大,孕早期的fT4呈上升趋势[152]。经允许,数据重绘自Okosieme等[44]的研究。 TSH检测 引言甲状腺激素和甲状腺激素受体的分子作用 TSH通常是甲状腺功能的一线检查并且优先于fT4[3]。TSH检测的优势反映了下丘脑- 垂体- 甲状腺轴的固有生理学,即相对于TSH的变化,fT4的微小变化会被放大100倍[45]。这种对数/ 线性的TSH/fT4关系,最初是在20世纪90年代用fT4指数法建立的[45],后来受到fT4类似物检测法研究的挑战[46],现已在直接fT4检测法中得到证实[47,48]。TSH/fT4的对数/线性关系表明,只有TSH测定才能检测出轻度(亚临床)甲状腺功能减退症或甲状腺功能亢进症。 TSH时代始于1927年,人们认识到垂体可分泌甲状腺刺激物[49]。早期检测使用耗费劳力的生物学方法,通过测定放射性标记小鼠或豚鼠甲状腺中TSH刺激的131碘-T4释放[50,51]。这些生物学方法还在甲状腺毒症患者的血清中发现了与TSH[52] 不同的异常长效甲状腺刺激物(longacting thyroid stimulator,LATS),现在被认为是导致Graves 病出现甲状腺功能亢进的TSH刺激性免疫球蛋白(TSH-stimulatingimmunoglobulin,TSI)[53]。早期的免疫学研究证明了TSH抗体的种属特异性,这与TSH放射免疫沉淀技术一起促使了第一代TSH RIA的发展[54,55]。 然而,由于TSH与促性腺激素具有同源性,这些早期的RIA与人绒毛膜促性腺激素(human chorionicgonadotropin,hCG)有交叉反应,因此需要加用hCG阻断剂[55],并且敏感性较差(约2.0 mIU/L),因此限制了它们用于诊断原发性甲状腺功能减退症[56]。在合成的促甲状腺激素释放激素(thyrotropin-releasinghormone,TRH)应用后[57],人们发现少量甲状腺激素可抑制TRH 刺激的TSH 释放[58],且TRH-TSH 的反应与基础TSH水平有关[59]。TRH兴奋试验的剂量和方案变得标准化,TRH刺激的TSH应答缺失成为甲状腺功能亢进症的诊断性试验[60],在此期间,由于检测方法不敏感,无法将基础TSH检测用于诊断[60]。 随后,检测的特异性得到了提高,TSH检测的“质量”成为该方法灵敏度的同义词,这可以在区分甲状腺功能亢进者和甲状腺功能正常者的TSH水平的能力上得到证明[60]。对提高TSH检测的敏感性的追求,使得试剂生产商采用了令人混淆的命名,如“ultRASensitive( 超灵敏)” 和“supersensitive( 超级灵敏)”作为营销策略来描述他们的TSH检测方法[60]。这促使科学界在临床实践中使用功能敏感性(functional sensitivity,FS)参数来反映检测的敏感性。对于TSH,FS定义为在具有临床实践代表性的时间跨度(6~8周)内,在批间CV为20% 的情况下,可在人血清中测定分析物的最低浓度[61]。2003年美国国家临床生物化学学会发布了FS的概念,同时推荐了其他甲状腺相关激素检测的FS方案[61]。 直至20世纪80年代,单克隆抗体(monoclonalantibody,mAb)的产生使TSH 检测发生了革命性的变化[62],促进了免疫测定法(immunometric assay,IMA)方法学的发展[63]。IMA本身比RIA更加敏感,尤其是用化学发光[64]或荧光[65]替代125碘同位素信号后。因此,更敏感的第二代(FS=0.1 mIU/L)、第三代(FS=0.01 mIU/L),甚至是研究中的第四代(FS=0.01 mIU/L)TSH检测方法不断被开发出来[45,60,66],而且越来越敏感,可以区分轻度(亚临床)和明显的甲状腺功能亢进症,且无需进行TRH。目前,TRH 检测的作用仅限于垂体功能评估[67]和TSH自身抗体(macro TSH)干扰的研究[68]。不过,尽管TRH在欧洲仍可获得使用,但目前在美国TRH尚未应用于临床。 目前,在大多数自动化仪器平台上使用的第三代TSH检测法可以诊断从甲状腺功能亢进到甲状腺功能减退的不同程度的原发性甲状腺功能异常[69]。非同位素IMA方法也被应用于新生儿先天性甲状腺功能减退症筛查的血斑检测[70]和床旁TSH检测[71]。 尽管检测灵敏度有了显著提高,并且使用了相同的人垂体提取物进行标准化(MRC 80/558),但目前的TSH方法在检测不同的TSH糖异构体(glycoisoforms)时存在特异性差异,并且并非所有的TSH糖异构体都具有生物活性。这些糖异构体由下丘脑TRH控制,受甲状腺功能减退等生理因素的影响,并且可使得分子构象改变而导致表位异常暴露或掩盖[72,73]。因此,不同检测方法报告的TSH 数值不同[43],这反映了用于每种IMA检测的专有mAb试剂识别表位特异性的差异。由于目前不同检测方法之间存在差异,无法为不同的生理状态如妊娠(图4)[44]和衰老[1]建立通用的参考范围。 x 图4. 汇总已发表的43项研究显示,使用不同方法(雅培、贝克曼、罗氏和西门子)在孕期各阶段检测的TSH参考上限和下限(2.5%~97.5%)。数据显示,正如所预期的一样,孕早期的TSH呈下降趋势,因为甲状腺受人绒毛膜促性腺激素的刺激并且在孕早期达峰[152]。经允许,数据重绘自Okosieme等[44]的研究。 此外,mAb IMA试剂不能区分具有免疫活性和生物活性的TSH,因此不能区分原发性或继发性(垂体或下丘脑)甲状腺功能障碍。因此,在中枢性甲状腺功能减退症中(其特征是分泌无生物活性的TSH亚型[74]、罕见的TSH β亚单位遗传变异[75]或分泌生物活性增强的TSH亚型的垂体瘤[76]),TSH的IMA测定可能具有诊断误导性。非TSH相关的干扰也仍然是问题所在。尽管检测制造商几乎已经将生物素干扰[41]完全消除,但要消除由于HAb(如人类抗小鼠抗体和类风湿因子)[77]、TSH自身抗体(macro TSH)[68]或针对IMA试剂的抗体(如钌和链霉亲和素)[41]造成的TSH水平虚高则更为困难。 甲状腺自身抗体(甲状腺球蛋白、抗微粒体/甲状腺过氧化物酶和TSH受体自身抗体) 引言甲状腺激素和甲状腺激素受体的分子作用 甲状腺球蛋白和抗微粒体/ 甲状腺过氧化物酶抗体 20 世纪50 年代中期,在观察到向兔子体内注射甲状腺腺叶提取物可诱导其产生甲状腺球蛋白自身抗体(thyroglobulin autoantibodies,TgAb),从而导致剩余甲状腺叶出现类似于桥本甲状腺炎的损伤后,人们摒弃了动物不能产生针对自身蛋白质的抗体这一观念[78,79]。早期检测TgAb和后来的抗微粒体抗体(antimicrosomalantibodies,AMA)[80]的方法是定性的,包括凝胶沉淀反应[78]、免疫荧光[81]和鞣质红细胞(tanned red cell,TRC)凝集反应[88]。到20世纪70年代末,定性TRC检测法被更敏感、更特异的定量竞争性结合放射分析法所取代[83],后者在Graves病、慢性甲状腺炎和其他自身免疫性疾病患者中报告了较高的阳性率。 已确认甲状腺过氧化物酶(thyroid peroxidaseenzyme,TPO)是微粒体抗原,AMA 检测就是TPO抗体(TPOAb)的检测[85]。随后,NHANE III调查使用TPOAb和TgAb的放射分析法评估了美国人群中的甲状腺抗体阳性率,并报告了在无明显甲状腺功能障碍的人群中,两种抗体的阳性率均约为10%[1]。抗体阳性的患病率随年龄增长而增加,尤其是女性,并受种族影响[1,86]。目前,仍有一些放射性检测方法,但大多数TgAb 和TPOAb 检测都是通过血清中的抗体与固相支持物上的抗原竞争结合,并通过非同位素信号进行检测[87]。 现今,该方法在与其他甲状腺检测相同的仪器平台上实现了自动化,并与来自美国国家生物标准和控制研究所的参考物(TgAb的MRC 65/093和TPOAb的MRC 19/260)进行了标准化。然而,目前的不同检测方法在敏感性、特异性和报告所用的度量数值方面各不相同[88]。与TgAb相比,TPOAb的方法间差异问题较小,这是因为TPOAb通常只检测一次,用于评估TSH 升高的病因[86] 或作为妊娠危险因素[86]。相比之下,对于检测TgAb对Tg测量的干扰[90],或以TgAb的变化趋势用作甲状腺癌的替代肿瘤标记物[91]来说,检测方法的灵敏度和特异性都至关重要。 TSH受体抗体 TBII检测不能提供TRAb是刺激性还是抑制性的功能状态信息。相反,生物活性分析表明,并非所有TRAb都刺激TSHR,一些TRAb能够抑制TSH的刺激,而其他TRAb结合TSHR,对TSH的作用是中性的[98]。在过去的40年中,TRAb功能上的这些差异导致了描述TRAb功能的术语词汇混乱不清[98]。刺激性TRAb的术语包括TSHR刺激性抗体或TSHR刺激性免疫球蛋白(TSAb或TSI),而抑制性TRAb的术语包括TSHR抑制性抗体或TSHR抑制性免疫球蛋白(TSB-Ab或TBI)。功能性TRAb的检测有助于研究桥本甲状腺炎和Graves 病的甲状腺外表现[98]。在妊娠患者中,TRAb特别有助于区分妊娠期一过性甲状腺毒症(无需治疗)或Graves病甲状腺毒症(需要治疗),并用于评估新生儿甲状腺功能减退症或甲状腺功能亢进症的风险[98]。 甲状腺球蛋白(Tg)检测 引言甲状腺激素和甲状腺激素受体的分子作用 给动物注射131碘的早期研究发现,Tg是一种含甲状腺素的碘蛋白,主要向甲状腺淋巴系统高浓度分泌,并在TSH刺激下增加[101-104]。这些研究证实,甲状腺是体内Tg的唯一来源,淋巴系统是其主要分泌途径。在随后的几十年里,Tg的甲状腺特异性起源被证实,促使人们将血清Tg测定作为甲状腺癌的肿瘤标志物。次要用途包括亚急性甲状腺炎和先天性甲状腺疾病的诊断。随着Tg基因定位于染色体8q24.2-q24.3并于1987年进行测序[105,106],高分子量(19S,660 kDa)的二聚体Tg糖蛋白的结构复杂性得到了广泛的研究[107]。最近应用冷冻电子显微镜技术已经阐明了人天然Tg经复杂的翻译后修饰的复杂蛋白结构[108-110]。 研究已经确定了Tg分子激素生成部位[111]和参与Tg分子成熟的过程,其中分子伴侣控制定点的糖基化、二聚化和分子折叠,这些过程对于在顶端细胞膜生成适合碘化的成熟Tg分子至关重要[107]。Tg生物合成过程的复杂性可导致分子异质性和构象异常。这种异常常见于以低碘含量[112,113]和异常糖基化[114-116]为特征的肿瘤性Tg。这种异常可能会改变Tg分子构象,掩盖或暴露可能与免疫检测试剂产生异常相互作用的表位,并改变Tg检测结果[117]。目前,使用不同方法检测同一血清样本,所报告的Tg数值存在显著差异,这可能反映了患者血清中Tg分子形式的异质性[117-119]。 20世纪20年代,血清中Tg首次在血液中检出是通过动物Tg抗体的沉淀反应[120]。20世纪50年代,区带电泳显示放射性碘治疗后Tg升高[121]。十年后,第一个直接测定Tg的RIA被开发出来,其灵敏度为约10 μg/L,只能检测到约60%的甲状腺功能正常的健康受试者的Tg[122]。然而,10年内RIA的敏感性提高了10倍(约1 μg/L),使得随后的病理生理学研究能够在大多数甲状腺功能正常的健康受试者中检测到Tg[123],并发现妊娠和脐血[124]中以及任何原因的甲状腺功能亢进症[123]中Tg水平升高。Tg在转移性分化型甲状腺癌(differentiated thyroid cancer,DTC) 患者中升高,成功治疗后降低,而在甲状腺髓样癌患者中未观察到Tg升高,这一发现巩固了血清Tg检测作为DTC肿瘤标志物的地位[125]。 第一代Tg 的RIA 方法[126,127]的敏感性欠佳,对未进行放射性碘清甲治疗患者无法检出持续性或复发性DTC[128]。此外,不同方法测定的血清Tg数值不同[129]。通过参照相同的人Tg 参考试剂(CRM-457)进行标准化,该问题得到了改善。然而,方法之间的差异依然存在,而且比持续使用相同方法的预期差异高出两到三倍(图5)[90],这可能是因为不同方法检测的是不同的Tg分子形式[118]。到2000 年,提高TgRIA检测灵敏度的努力与提高TSH检测灵敏度的努力不谋而合。重组人促甲状腺激素(recombinant humanTSH,rhTSH)[131,132] 被用于刺激基础Tg达到可测量范围的10倍,就像20年前TRH刺激的TSH被用于增加TSH检测的灵敏度一样[59]。 图5. 34例TgAb阴性的转移性分化型甲状腺癌患者血清Tg 测量结果的方法间变异性。患者有颈部淋巴结转移(空心圆)或远处转移(实心框)。图a,血清Tg低范围水平(<40 lg/L);图b,血清Tg高范围水平(>40 lg/L)。检测方法为IMA(贝克曼公司)、LCMS/MS(MS)方法(梅奥医学实验室)和RIA(南加州大学内分泌实验室)。数据摘自Spencer 等的研究[90]。IMA,免疫测定法;LCMS/MS,液相色谱法/串联质谱法;RIA,放射免疫分析法。 然而,2000年至2010年期间,基于免疫化学发光法(immunochemiluminometric,ICMA)的第二代Tg检测方法出现了[133]。与RIA 相比,ICMA 本身具有更高的灵敏度(FS=0.1 μg/L)[133],并避免了昂贵和不方便的rhTSH刺激[134,135]。目前,几乎所有用于内分泌检测的自动化仪器平台都可以进行第二代ICMA检测。然而,由于TgAb在DTC中的阳性率是一般人群的2倍[1,136],所有Tg IMA方法的主要局限性仍然是TgAb的干扰,导致结构性DTC患者的Tg IMA结果虚低或检测不到[88,90,137,138]。 20世纪50年代末,人们在血清中鉴定出TgAb[78],并证明TgAb可与125碘-Tg结合。由此可见,TgAb干扰引起的Tg RIA结果虚高是RIA 检测一开始就公认的问题。因此,含有TgAb 的血清通常被排除在Tg研究之外[122,139]。1978年,确定了TgAb干扰RIA法检测程度和方向的决定因素[140]。为此,优化一些RIA方法,采用高比放射性的125碘-Tg示踪剂和高亲和力的多克隆抗体以减少干扰[126,127,136,141]。2008年,以克服TgAb干扰为目标开发了第一个LC-MS/MS Tg检测方法[142]。 目前,虽然市面上有4种LC-MS/MS Tg检测方法[138,143-145],但LC-MS/MS方法是否不受TgAb干扰仍存在争议,因为有研究报道,约40%的TgAb阳性的结构性病变DTC患者在LC-MS/MS检测中检测不到Tg[90,138,146]。然而,无论使用何种方法检测Tg(RIA、IMA 或LC-MS/MS),灵敏的TgAb检测仍然是解释Tg检测结果的关键[88]。事实上,近年来TgAb 变化趋势已被公认为是TgAb阳性DTC患者的替代肿瘤标志物[91,147]。除了持续存在的TgAb干扰问题外,监测Tg和TgAb趋势作为DTC肿瘤标志物的临床应用仍然受到当前Tg[119]和TgAb[148]检测方法间差异的负面影响。这就需要最好是在同一实验室使用同一厂家的方法对DTC 患者进行(Tg和TgAb)监测[147]。 讨论 引言甲状腺激素和甲状腺激素受体的分子作用 1895年,Magnus-Levy发现甲状腺分泌物促进人类的基础代谢率(basal metabolic rate,BMR)[149,150],而他自己的BMR随着年龄的增长而下降。这些研究促使了将BMR作为甲状腺功能最早的检查。在此后的140年里,研究阐明了调控下丘脑- 垂体- 甲状腺轴的因素[151],以及累及美国约10%人口的甲状腺疾病的病因[1]。甲状腺疾病患者大多在门诊接受治疗,且60%的内分泌实验室检查产生于此[3]。未来的研究方向可能包括如何消除检测干扰和使用国际验证的参考试剂实现测试的标准化或协调化。消除与方法相关的变异性将有助于建立通用的参考范围。


20世纪50年代,唯一的甲状腺功能检测是以蛋白结合碘(protein-bound iodine,PBI)的形式估计总甲状腺素(total thyroxine,TT4)水平。PBI主要反应血清T4浓度,对T3也有一定作用。血清蛋白沉淀后灰化,用比色法测定碘化物含量[16]。这些PBI的检测通常使用高温和强酸,且气味难闻,同时容易受到含碘治疗化合物的干扰。20世纪70年代,实验室人员能够便利地使用放射免疫分析法(radioimmunoassay,RIA)替代PBI化学检测,使用阻滞剂减弱甲状腺激素与血浆蛋白的结合,促进激素与多克隆抗体试剂的结合,进而对TT4、总三碘甲腺原氨酸(total triiodothyronine,TT3)及后来的rT3 进行检测[17-19]。随后,通过放射免疫学检测干血样本中的T4开启了新生儿甲状腺功能减退症的第一次大规模筛查项目[20]。
70多年前提出的游离激素假说指出,当激素与血浆蛋白结合时,只有部分游离激素[0.03%的fT4和0.3%的游离三碘甲腺原氨酸(free triiodothyronine,fT3)] 具有生物学活性,可以进入组织发挥激素的作用[30,31]。遗憾的是,皮摩尔范围内的fT4检测带来了相当大的技术挑战,这促使人们持续50年寻求快速、直接的fT4检测方法,这些方法无需使用平衡透析[32,33]、超滤[34]或柱层析[35]等劳动强度大、成本高的方法将游离激素与结合激素进行物理分离。
在20世纪80年代, 建立了一系列fT4和fT3“估测”方法来取代两步指数方法。这些方法的有效性取决于在分析过程中尽量减少TBG的影响,同时保持游离和结合激素之间的平衡,也就是说,在分析过程中,应该只有最小限度的与TBG结合的T4解离成游离状态。这些方法使用了两种不同的创新免疫测定方法。
这些竞争性免疫分析法使用标记的T4类似物(如T4- 白蛋白偶联物)或标记的抗体与血清中的游离激素竞争有限数量的固相抗体结合位点[37]。尽管这些方法在消除TBG的影响方面相当成功,但它们因对白蛋白异常(如家族性异常白蛋白致高甲状腺素血症和无白蛋白血症)、其他异常甲状腺激素结合蛋白(如T4和T3自身抗体)[37]以及非酯化脂肪酸和一系列从TBG上置换出T4药物的干扰过于敏感而受到诟病[24,38]。
在这些方法中,血清中的fT4与有限数量的固相T4抗体发生反应[29,39]。洗脱未结合的血清成分后,使用标记的配体定量未占据的抗体结合位点。由于洗脱步骤去除结合蛋白,因此与类似物检测形式相比,这种方法设计似乎不太容易受到异常结合蛋白的影响[40]。
TRAb最初是作为TSH生物检测中异常的LATS被发现的[51,92],后来被证明是靶向TSH受体(TSHreceptor,TSHR)的自身抗体,是导致Graves甲亢及其甲状腺外表现的自身抗体[93]。第一个TRAb检测使用竞争性结合分析,测定血清中作为甲状腺结合抑制免疫球蛋白(thyroid-binding inhibiting immunoglobulins,TBII)的TRAb,TBII可抑制标记的TSH与人或豚鼠甲状腺细胞膜结合[53,94,95]。最近,与TSHR结合的mAb取代了标记的TSH,甲状腺细胞膜也被纯化的TSHR制剂[94,96]或克隆的TSHR所取代[97]。目前的TBII检测大多是自动化、非同位素的,并有国际参考试剂(MRC 65/122)进行标准化[94,98]。TRAb生物测定已经从耗费劳力的以FRTL-5细胞为基础的方法(需要提取IgG并以RIA测定的cAMP 为终点)[99],发展到使用含有转染重组TSHR和cAMP依赖性发光信号的中国仓鼠卵巢细胞[100]。